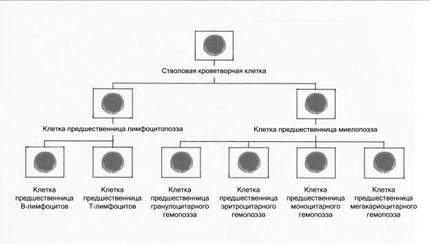
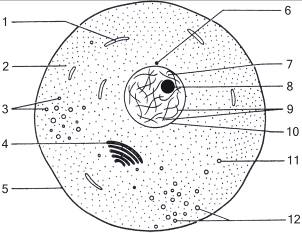
Книга: Мононуклеарный онкогенезКнига: Мононуклеарный онкогенезМОНОНУКЛЕАРНЫЙ ОНКОГЕНЕЗ Введение злокачественный мононуклеарный заболевание лечение Онкогенез (греч. onkos – масса, нарост, опухоль; genesis – развитие) – многоступенчатый механизм возникновения, роста и развития злокачественного процесса. Согласно вышеуказанному определению онкогенез состоит из трех основных процессов, причем каждый последующий – есть результат предыдущего, каждый имеет свои отличительные особенности и онкогенез может закончиться на каждом из них. В современной онкологии наиболее спорным является основной или фундаментальный вопрос – природы злокачественного процесса, т. к. до сих пор продолжаются споры о происхождении злокачественных клеток. Мы не надеемся охватить всю проблему онкогенеза, да это в принципе и не возможно сделать. Наша задача создать простую доступную для понимания универсальную теорию, где многие признанные факты нашли бы свое место. 1. Злокачественная клетка В доступной литературе имеются описания молекулярно-генетических механизмов онкогенеза. Попробуем суммировать и проанализировать основные его положения: 1-я стадия (инициации) – под канцерогенным воздействием (ионизирующее излучение, эндо- и экзоканцерогены, вирусы) наряду с относительно нейтральными повреждениями генома, могут происходить значимые мутации в онкогенах и антионкогенах. При этом возникает характерный спектр нарушений на генном, хромосомном и геномном уровнях: амплификации (увеличение копийности генов), делеции, инсерции, транслокации, микромутации (точковые замены, микроделеции, микроинсерции) и др. Условия инициации: – инициатор (ионизирующее излучение, эндо- и экзоканцерогены, вирусы) должен быть применен однократно и кратковременно, причем от дозы инициатора зависит частота возникновения злокачественного процесса – чем сильнее, тем вернее; – инициация может происходить только во время митоза клетки, т.е. в зоне естественной интенсивной пролиферации соматических клеток; – более вероятно, что инициация произойдет в зоне с хронически усиленной пролиферацией, стимулированной внешним или внутренним влиянием, т.е. определенные хронические процессы в организме-носителе, должны постоянно поддерживать усиленную пролиферацию соматических клеток; – инициация необратима, т.е. нарушения на генном, хромосомном и геномном уровнях нельзя восстановить до нормального состояния; – инициация должна полностью прекратиться и только после этого может воздействовать промотор, т.е. необходимо изменение условий нахождения клетки: инициация должна происходить, когда клетка находится в одних условиях, а дальнейшее воздействие на клетку (промоция), когда клетка с измененным генотипом находится уже совершенно в других условиях существования и микроокружения; – учитывая, что в злокачественной клетке проявляются эмбриональные черты, то пролиферирующая зона должна иметь свое начало с эмбрионального периода развития организма, а также в период трансформации нормальной пролиферирующей соматической клетки в злокачественную клетку должны быть созданы условия, подобные эмбриональным; – известно, что злокачественные клетки имеют различный уровень потентности: от унипотентной до полипотентной, т.е. уровень потентности клетки-предшественницы в процессе трансформации в первичную стволовую злокачественную клетку должен быть достаточно высоким – унипотентный или полипотентный; – Шимке Р.Н. (1981): минимальная частота злокачественных новообразований передаваемых по наследству составляет в среднем 7% (1–15% по данным разных авторов, по различным онкологическим заболеваниям), т.е. в среднем в 7% случаев, возникают злокачественные заболевания, передаваемые по наследству «кровным» родственникам. Здесь этап инициации не обязателен, необратимые изменения генотипа ядерной ДНК уже переданы по наследству. Таким образом, однократное и кратковременное канцерогенное воздействие, приводит к необратимым генотипическим изменениям ядерной ДНК пролиферирующей соматической клетки. Однако для «зарождения» стволовой злокачественной клетки одной инициации недостаточно. 2-я стадия (промоции): генотипически измененная клетка подвергается воздействию промотора в условиях отличных от первоначального состояния. В первую очередь, воздействию подвергаются клеточная мембрана и цитоплазма. Структурные изменения клеточной мембраны и химические изменения в цитоплазме клетки, влияют на проявление генотипических изменений ядерной ДНК – эпигенетический механизм. Условия промоции: – промоция эффективна только после инициации и, более того, после полного прекращения воздействия инициатора, т.е. инициированная клетка должна находиться в других условия существования и микроокружения; – интервал между инициацией и промоцией не влияет на конечную частоту злокачественных новообразований, т.е. продолжительность жизни инициированной клетки может быть вариабельный, но желательно, как можно дольше (месяцы, годы); – промотор должен воздействовать на инициированную клетку длительно и непрерывно, т.е. инициированная клетка с продолжительным жизненным циклом должна находиться в определенных изолированных условиях, когда агрессивное воздействие на нее может продолжаться сравнительно долго (месяцы, годы); – промотор должен оказывать многообразное влияние на инициированную клетку: структурную организацию клеточной мембраны с изменением ее избирательной проницаемости, химическое состояние цитоплазмы, клеточную дифференцировку, возможность блока межклеточных связей и др.; – промоция обратима в начале стадии, т.е. начальные проявления воздействия промотора, могут исчезнуть, и клетка вернется к своему инициированному состоянию; – Варбург О.Г. (1956): злокачественные клетки возникают путем отбора при нарушении дыхания нормальных клеток, в условиях с низким содержанием кислорода или бескислородной среде. Большинство клеток в этих условиях погибают, а те, которые в процессе отбора изменяют свой обмен в сторону интенсивного гликолиза, т.е. бескислородного освобождения энергии – выживают, размножаются и через ряд поколений образуют злокачественный очаг. Таким образом, пролиферирующая соматическая клетка, имеющая генотипические изменения ядерной ДНК, попадает в «суперусловия», где подвергается длительному и непрерывному (месяцы, годы) агрессивному воздействию в условиях бескислородной среды. В результате она приобретает эпигенетические изменения – структурные нарушения клеточной мембраны и химические изменения в цитоплазме. В настоящее время считается, что генотипические и эпигенетические изменения пролиферирующей соматической клетки, являются подготовительными и, в тоже время, пусковыми к механизму собственно трансформации в стволовую злокачественную клетку. Непременным условием для осуществления механизма трансформации является достаточная изоляция от влияния организма-носителя. 2. Злокачественные заболевания Все злокачественные заболевания человека подразделяются на две основные группы: гемобластозы и солидные опухоли. Принцип подразделения основан на различной локализации злокачественного процесса и известной схожести злокачественных клеток с нормальными клетками микроокружения. Вопрос о происхождении злокачественных заболеваний остается спорным, несмотря на имеющуюся большую информацию и многочисленные фактические данные. И если ранее говорили о гистогенезе – тканевом происхождении, то сейчас уже можно говорить о цитогенезе – клеточном происхождении злокачественных новообразований. Считается наиболее изученным цитогенез злокачественных заболеваний кроветворной и лимфоидной ткани, в основе которого положено учение о стволовых и полустволовых клетках-предшественниках кроветворения. Цитогенез солидных опухолей до сих пор не изучен, нет четкого представления из каких клеток-предшественников возникают злокачественные клетки. Именно поэтому мы и будем рассматривать в основном вопросы, касающиеся солидных опухолей, проводя возможную аналогию с гемобластозами. Общие признаки гемобластозов и солидных опухолей: 1. Этиология: химические вещества (эндо- и экзоканцерогены), ионизирующее излучение, вирусы. 2. Патогенез: генотипические изменения ядерной ДНК и эпигенетические изменения – нарушения структуры клеточной мембраны и химические процессы в цитоплазме клетки с появлением новых свойств или переписывание информации с ДНК/РНК вируса на геном клетки, что в конечном итоге приводит к возникновению признаков злокачественного роста. 3. Диагностика: клиника, лабораторные и инструментальные методы исследования с обязательным морфологическим подтверждением диагноза (гистологическое или цитологическое исследование). 4. Осложнения: инфекционные, тромботические, нарушение нормального механизма костеобразования, желудочно-кишечные осложнения (тошнота и рвота, икота, задержка стула, диарея, мукозиты), интоксикация, психические изменения (тревога, депрессия, агрессивные реакции, суициды). 5. Принципы патогенетической терапии: воздействия подавляющие пролиферацию злокачественных клеток (рентгеновское облучение, химиотерапия, гормонотерапия, иммунотерапия), витаминная терапия, вспомогательная терапия (переливание крови, купирование инфекции, терапия тромбозов и кровотечений), трансплантация костного мозга. 6. Причины смерти: кахексия, присоединившаяся инфекция, тяжелая анемия, тромбоэмболические осложнения, массивные кровотечения и кровоизлияния. 7. Основные признаки злокачественности: передача всех свойств по наследству, сохранение принципа злокачественной прогрессии, бесконтрольное деление клеток, инвазивный рост, метастазирование. Таким образом, общая схожесть гемобластозов и солидных опухолей заложена на генетическом уровне. Различия между гемобластозами и солидными опухолями Рассмотрим каждую группу злокачественных заболеваний в отдельности, при этом гемабластозы разделим на две подгруппы: лейкозы и лимфомы. На основании изучения «начала» всех злокачественных заболеваний, можно сделать следующие выводы: 1. Лейкозы – это многочисленная разнородная группа злокачественных заболеваний, развивающихся из гемопоэтических (кроветворных) клеток поражающих красный костный мозг: – клетками-предшественниками стволовых злокачественных клеток являются полипотентные или унипотентные стволовые клетки очагов миело- или лимфопоэза в красном костном мозге; – обе стадии (инициации и промоции) «зарождения» стволовой злокачественной клетки происходят в одном месте – в красном костном мозге; – основой «зарождения» стволовой злокачественной клетки является блок дифференцировки и трансформация полипотентной или унипотентной стволовой клетки миело- или лимфопоэза; – механизм «зарождения» стволовой злокачественной клетки заключается в генотипических и эпигенетических изменениях полипотентной или унипотентной стволовой клетки миело- или лимфопоэза, под канцерогенным воздействием; – начинается злокачественный процесс с «зарождения» одной стволовой злокачественной клетки, которая затем формирует клон злокачественных клеток; – проявляется заболевание развитием злокачественного процесса в красном костном мозге, при этом первичный злокачественный очаг отсутствует; – развивается злокачественный процесс за счет пролиферации злокачественных клеток в пределах красного костного мозга, гематогенного и лимфогенного распространения по организму-носителю; – влияет злокачественный процесс на гемопоэз, гомеостаз, иммунитет и т.д. 2. Лимфомы – это группа злокачественных гематологических заболеваний лимфатической ткани, характеризующихся злокачественной трансформацией лимфоидных клеток: – клетками-предшественниками стволовых злокачественных клеток являются полипотентные или унипотентные стволовые клетки лимфопоэза в красном костном мозге; – 1-я стадия (инициации) «зарождения» стволовой злокачественной клетки происходит в красном костном мозге, 2-я стадия (промоции) – в месте организации первичного злокачественного очага; – основой «зарождения» стволовой злокачественной клетки является блок дифференцировки и трансформация полипотентной или унипотентной стволовой клетки лимфопоэза; – механизм «зарождения» стволовой злокачественной клетки заключается в генотипических и эпигенетических изменениях полипотентной или унипотентной стволовой клетки лимфопоэза, под канцерогенным воздействием; – начинается злокачественный очаг с «зарождения» одной стволовой злокачественной клетки, которая затем формирует клон злокачественных клеток; – проявляется злокачественный процесс организацией первичного злокачественного очага, располагающегося в лимфатических узлах (нодальное поражение) или в любых других органах и тканях (экстранодальное поражение); – развивается злокачественный процесс за счет лимфогенного распространения по организму-носителю, иногда клетки лимфомы находят в крови, но обычно они имеют тенденцию формировать плотные опухоли в лимфатической системе или внутренних органах (печени, желудке, нервной системе или в других местах); – влияет злокачественный процесс на гемопоэз, гомеостаз, иммунитет и т.д. 3. Солидные опухоли – наибольшая в количественном отношении, разнородная группа злокачественных заболеваний, развивающихся в результате многоступенчатой злокачественной трансформации нормальной пролиферирующей соматической клетки в стволовую злокачественную клетку: – происхождение злокачественных клеток не известно, т.е. не известна клетка-предшественница стволовой злокачественной клетки. Предполагают, что клетками-предшественниками являются нормальные соматические пролиферирующие клетки – камбиальные клетки, расположенные в области дна крипт, шейке желез, надкостнице, надхрящнице и по ходу кровеносных сосудов, в зоне интенсивной восстановительной пролиферации; – где и как происходят обе стадии (инициации и промоции) «зарождения» стволовой злокачественной клетки, не известно. Предполагают – в зоне интенсивной пролиферации клеток; – какой процесс лежит в основе «зарождения» стволовой злокачественной клетки, не известно. Предполагают, что происходит трансформация нормальной пролиферирующей соматической клетки в стволовую злокачественную клетку; – каков механизм «зарождения» стволовой злокачественной клетки, не известно. Предполагают, что при канцерогенном воздействии происходят генотипические и эпигенетические изменения нормальной пролиферирующей соматической клетки, которые и являются пусковым механизмом к ее трансформации в стволовую злокачественную клетку; – начинается злокачественный очаг с «зарождения» одной стволовой злокачественной клетки (80%), двух или более стволовых злокачественных клеток (20%), которые затем формируют клон злокачественных клеток; – проявляется злокачественный процесс организацией первичного злокачественного очага, располагающегося в различных органах и тканях, увеличение которого происходит за счет пролиферации клеток, аппозиционного и инвазивного роста; – развивается злокачественный процесс за счет гематогенного и лимфогенного распространения по организму-носителю с организацией вторичных очагов – метастазов; – влияет злокачественный процесс на гемопоэз, гомеостаз, иммунитет и т.д. Таким образом, согласно современным представлениям: 1. Разница между гемобластозами (лейкозы и лимфомы) с одной стороны и солидными опухолями – с другой, заключается в основе и механизме «зарождения» стволовой злокачественной клетки: – при гемобластозах, под канцерогенным воздействием возникают генотипические и эпигенетические изменения полипотентной или унипотентной стволовой клетки миело- или лимфопоэза, блок дифференцировки и трансформация ее в стволовую злокачественную клетку; – предполагают, что при солидных опухолях под канцерогенным воздействием происходят генотипические и эпигенетические изменения нормальной пролиферирующей соматической клетки, которые и являются пусковым механизмом к ее трансформации в стволовую злокачественную клетку. 2. Разница между лейкозами с одной стороны, лимфомами и солидными опухолями – с другой, заключается в проявлении злокачественного процесса: – при лейкозах заболевание проявляется поражением красного костного мозга, первичный злокачественный очаг не организуется. Для «зарождения» стволовой злокачественной клетки необходимо 2–4 генотипических изменений ядерной ДНК полипотентной или унипотентной стволовой клетки миело- или лимфопоэза. Эпигенетические изменения имеют второстепенное значение, поэтому смена условий существования и микроокружения клетки-предшественницы стволовой злокачественной клетки не являются обязательными; – при лимфомах и солидных опухолях заболевание проявляется обязательной организацией первичного злокачественного очага. Для «зарождения» стволовой злокачественной клетки необходимо 7–8 генотипических изменений ядерной ДНК клетки-предшественницы стволовой злокачественной клетки. Генотипические и эпигенетические изменения имеют равноценное значение, поэтому смена условий существования и микроокружения клетки-предшественницы являются обязательными. Большее число генотипических изменений ядерной ДНК, а также равноценное значение генотипических и эпигенетических изменений определяют длительность предклинического развития заболевания. 3. Характер опухолевого роста лимфом имеет общие черты, как с солидными опухолями – организуют первичный злокачественный очаг и метастазирование, так и с лейкозами – способны формировать состояния, напоминающие лимфоидный лейкоз. Поэтому лимфомы относят к промежуточному варианту развития злокачественного процесса. 4. Учитывая, что при гемобластозах 1-я стадия (инициации) «зарождения» стволовой злокачественной клетки происходит в красном костном мозге, то логично предположить, что и при солидных опухолях 1-я стадия (инициации) клетки-предшественницы стволовой злокачественной клетки, также происходит в красном костном мозге. Тогда последующая 2-я стадия (промоции) происходит в органах и тканях, где происходит «зарождение» стволовой злокачественной клетки и организуется первичный злокачественный очаг. 3. Предпосылки мононуклеарного онкогенеза Для создания теории «Мононуклеарного онкогенеза» как естественного механизма возникновения, роста и развития злокачественного процесса мы посчитали возможным подвергнуть сомнению существующую теорию о происхождении первичной стволовой злокачественной клетки солидных опухолей из камбиальных клеток покровного или железистого эпителия. Ведь вопрос о том, из какого клеточного и / или тканевого субстрата происходят стволовые злокачественные клетки солидных опухолей, до сих пор является дискуссионным и до настоящего времени точно не определен круг клеток, которые могли бы претендовать на роль клетки-предшественницы первичной стволовой злокачественной клетки. В этом случае сразу же возникают два вопроса: Вопрос 1. На основании, какого фактического материала может быть высказано сомнение о происхождении первичной стволовой злокачественной клетки из камбиальных клеток покровного или железистого эпителия? Ответ: 1. Теоретически любая соматическая клетка может превратиться в злокачественную клетку. Однако отождествлять процессы трансформации in vitro и онкогенность клеток in vivo нельзя, т. к. превращение нормальной клетки в злокачественную клетку есть процесс, инициируемый на молекулярном уровне и включающий последовательную работу нескольких групп генов, причем онкогенам принадлежит ключевая роль, заключающаяся в «запуске» этих процессов. 2. Злокачественный процесс возникает не сразу, ему предшествуют патологические изменения, которые при определенных условиях приводят к развитию злокачественного заболевания. Это касается процессов, характеризующихся тканевым ростом, и такие состояния называются предраковыми. Понятие «предрак» охватывает изменения клинического, морфологического (структурного), цитологического (клеточного) и биохимического характера. Часто это хронические воспалительные и дистрофические изменения. 3. При возникновении и развитии злокачественного процесса, следует иметь в виду не только местные патологические изменения ткани, но и общие заболевания организма. Опухоль возникает в том или другом органе или ткани, в том или ином месте, начинаясь с появления опухолевого «зачатка» или злокачественного «зародыша», который вначале состоит из небольшой группы изменившихся и продолжающих изменяться клеток. Появление такого «зародыша» может быть обусловлено различными воздействиями, влияющими не только местно, но и на организм в целом. 4. Шарай Л.А. и соавт. (1961): эксперимент на желудке кошек – путем ежедневного в течение года введения в желудок молока или мясного бульона имевших температуру 59–61 град. С воспроизводили хронический воспалительный и регенеративный процесс подобный состоянию эпителия, который встречается при раковом состоянии желудка человека (у кошек рака желудка не бывает). Однако при прекращении агрессивного воздействия эпителий желудка постепенно приходил в норму. Вывод: гиперплазия и анаплазия эпителия не приводит к его трансформации в злокачественную клетку. 5. Cornil A.V. (1908): описал схожесть клеток инвазивного рака с клетками эпителия протоков. Однако предположение, что злокачественные клетки возникают из эпителиальных клеток, до сих пор дискутируется. На сегодняшний день однозначно можно сказать, что гиперплазия и метаплазия эпителия не приводит к малигнизации. При этом дисплазия эпителия уже рассматривается, как злокачественный эпителий, происхождение которого не ясно. 6. Сведения о самых ранних изменениях в эпителиальных клетках, как клетках-предшественниках злокачественных клеток, ограничиваются представлением об отсутствии предопухолевого состояния, которое было бы общим для всех видов рака и скудными данными о ранних стадиях различных злокачественных заболеваний. 7. Атипический поверхностный эпителий является неустойчивой кратковременной структурой, он легко отторгается и чаще вновь не образуется, т.е. восстановительная способность выражена очень слабо. Это приводит к тому, что малигнизированные участки слизистой оболочки часто лишены эпителиальной выстилки и на раневой поверхности скапливается значительное количество детрита, образованного погибшими элементами. 8. Turkington (1972): в норме эпителиальные клетки молочной железы под влиянием инсулина, гидрокортизона и пролактина дифференцируются в секреторные альвеолярные клетки. При мышином раке молочной железы злокачественные клетки не реагируют на эти гормоны клеточной дифференцировки. 9. Райхлин Н.Т. (1975): единым источником возникновения злокачественных клеток являются камбиальные клетки (стволовые клетки или клетки-предшественники) сохранившие в процессе малигнизации в определенной степени способность к дифференцировке. Однако ни одним свойством, которым обладают злокачественные клетки, не обладают эпителиальные клетки и ни одна функция эпителия (покровная, защитная, экзокринная), не передалась злокачественным клеткам. 10. При малигнизации нормальных тканей взрослого организма не удается проследить постепенного перехода от нормальных тканей к малигнизированным и не удается гистологическими и цитологическими методами исследования найти переходных клеток между нормальными клетками микроокружения и злокачественными клетками. 11. Рак желудка: до настоящего времени не установлено, что следует считать началом малигнизированного роста в слизистой оболочке, какое строение при этом имеет эпителий. Основные признаки дифференцировки эпителия – секреторная деятельность и гетерополярность при злокачественном процессе нарушены. Злокачественные клетки рака желудка с высокой частотой экспрессируют фактор, ингибирующий миграцию макрофагов, что не характерно для нормальных эпителиальных клеток слизистой желудка. Первичные злокачественные клетки расположены в пределах слизистой, вторичные злокачественные клетки врастают в слизистую оболочку из подслизистой. 12 Рак легкого: в эксперименте признаются два источника происхождения злокачественных клеток первичного рака легкого – эпителий бронхов и выстилка альвеол, хотя дифференцировать злокачественные клетки того и другого новообразования не представляется возможным. 13. В «предраковой» печени возникают фокальные очаги регенерации, состоящие из морфологически и гистохимически однородных гепатоцитов. Узелки очень напоминают образование клональных кроветворных колоний в селезенке облученных животных. Нет доказательств, что они возникают из овальных клеток или юных гепатоцитов. При прекращении канцерогенного воздействия гиперпластические узелки утрачивают свою обособленность и входят в структуру нормальной печени. Какие клетки-предшественники являются основой для образования клональных кроветворных колоний в предраковой печени – не известно. 14. Первичный рак печени: считается, что злокачественные клетки могут исходить из эпителиальных клеток паренхимы – гепатома (гепатоцеллюлярный рак) или из эпителия желчных путей – холангиома (холангиоцеллюлярный рак), хотя дифференцировать злокачественные клетки того и другого новообразования не представляется возможным. 15. Образование злокачественных клеток в коже, пищеводе и прямой кишке идет весьма сходно и малигнизированное состояние этих клеток не имеет большого разнообразия. 16. В метастазах меланомы клеточные элементы демонстрируют крайнюю степень нарушения дифференцировки, решающим признаком остается пигментное включение – меланин. 17. Темпы роста злокачественного очага отличаются чрезвычайно большим диапазоном и не зависят от органной принадлежности, его морфологического строения и количества митозов в злокачественной ткани. 18. «Зарождению» злокачественных клеток способствуют среды, резко отличные от нынешней среды обитания нормальных клеток. Несомненно, первые злокачественные клетки не обладают той степенью совершенства, что свойственна окружающим их нормальным клеткам. Однако, по-своему злокачественные клетки совершенны, а в дальнейшем в результате злокачественной прогрессии степень их совершенства повышается, что является результатом эволюции. 19. Считается, что злокачественные клетки различных органов и тканей солидных опухолей происходят из разных зародышевых листков, однако принципы возникновения, роста и развития злокачественного процесса совершенно идентичны. 20. На основании морфологических данных обычно указывают, что злокачественное новообразование, особенно отличающееся от тканей микроокружения, одновременно является и наиболее злокачественным. 21. Злокачественный процесс развивается по определенной программе и общим правилом является известное постоянство его индивидуальной структуры в течение всех периодов возникновения, роста и развития. 22. Характерные морфологические особенности данной формы злокачественного новообразования большей частью уже определены в злокачественном «зародыше». Существуют многочисленные отклонения от этого правила с эволюцией структуры злокачественного новообразования, то в сторону более дифференцированного, то (чаще) в сторону менее дифференцированного строения. 23. Имеются фенотипические и генотипические различия между злокачественными клетками лейкозов, лимфом и солидных опухолей, между злокачественными клетками одной группы и даже между злокачественными клетками в одном злокачественном новообразовании, но по основным характеристикам злокачественные клетки одинаковы. 24. Важные и никем неоспоримые утверждения: – злокачественные клетки имеют больше сходства между собой, чем нормальные клетки между собой; – злокачественные клетки имеют меньше различий между собой, чем различия между злокачественными клетками и нормальными клетками; – нормальные клетки имеют меньше различий между собой, чем различия между нормальными клетками и злокачественными клетками; – основные принципы «зарождения» злокачественной клетки, роста первичного очага и развития злокачественного процесса различных органов и тканей совершенно идентичны. 25. И многое другое. Таким образом, на основании вышеизложенного можно высказать определенное сомнение о происхождении первичной стволовой злокачественной клетки из камбиальных клеток покровного или железистого эпителия. Вопрос 2. Какая клетка может претендовать на роль «общего начала» или клетки-предшественницы первичной стволовой злокачественной клетки солидных опухолей? Ответ: Истоки «зарождения» первичной стволовой злокачественной клетки солидных опухолей необходимо искать не среди местных клеток непосредственного окружения первичного злокачественного очага, как это безуспешно пытаются делать на протяжении многих десятилетий, а в долгой эволюционной предыстории и эмбриональном периоде развития организма-носителя, рассматривая среды, резко отличные от прежней среды обитания клеток-предшественников. При анализе всех клеток организма человека необходимо выбрать, прежде всего, те клетки, которые имеют следующие основные свойства: 1. Являются соматическими пролиферирующими клетками с продолжительным жизненным циклом (месяцы, годы). 2. Обладают автономностью: умеют свободно перемещаться по всему организму-носителю, проникать и мигрировать в органах и тканях. 3. Способны влиять на различные жизненно важные процессы: гемопоэз, гомеостаз, иммунитет, пролиферацию, созревание и дифференцировку клеток и др. Клетками, обладающими вышеуказанными свойствами, в организме человека являются только клетки системы крови. Из всех клеток системы крови на роль «общего начала» или клетки-предшественницы первичной стволовой злокачественной клетки солидных опухолей могут претендовать только Мононуклеары (от лат. monos – один и nucleus – ядро). Для этого утверждения есть все основания: – только Мононуклеары (Промоноциты и Моноциты) являются соматическими пролиферирующими клетками; – только Мононуклеары имеют продолжительный жизненный цикл (месяцы и годы), все остальные клетки крови короткоживущие – быстро заканчивают свой жизненный цикл; – только Мононуклеары обладают достаточной автономностью: умеют свободно перемещаться по всему организму-носителю током крови, проникать и мигрировать в различных органах и тканях; – только Мононуклеары (Промоноциты, Моноциты) в красном костном мозге и кровеносном русле являются промежуточным вариантом развития, а в тканях трансформируются в Макрофаги, все остальные клетки крови являются тупиковым вариантом, без какой-либо возможности на дальнейшее развитие; – только Мононуклеары имеют большие полномочия и возможности влиять на различные жизненно важные процессы, протекающие в макроорганизме: гемопоэз, гомеостаз, иммунитет, пролиферацию, созревание и дифференцировку клеток и др.; – только Мононуклеары могут принимать фенотип клеток микроокружения – мезенхимально-эпителиальный переход. Таким образом, Мононуклеар – клетка, которая может претендовать на роль «общего начала» или клетки-предшественницы первичной стволовой злокачественной клетки солидных опухолей. 4. Формирование «предопухолевого» ложа Возникновению злокачественного процесса предшествуют предопухолевые заболевания организма в целом и патологические изменения местных тканей в частности. Процесс сопровождается структурной перестройкой органа и / или ткани, формированием оптимальных условий для возникновения, роста и развития злокачественного процесса и неблагоприятных условий для нормальных клеток и тканей микроокружения. 1. ПРЕДОПУХОЛЕВЫЕ ЗАБОЛЕВАНИЯ ОРГАНИЗМА Предопухолевые заболевания – это общее название врожденных и / или приобретённых изменений тканей, способствующих возникновению, росту и развитию злокачественного процесса. Различают С клинической точки зрения различают облигатные и факультативные предопухолевые заболевания: 1. Облигатные (обязательные) – патологические изменения ткани, обусловленные генетическими или врождёнными факторами, которые обязательно перерождается в злокачественное заболевание: семейный полипоз толстой кишки, пигментная ксеродерма, дерматоз Боуэна, аденоматозный полип желудка, некоторые виды мастопатии, некоторые доброкачественные опухоли. Время возникновения злокачественного новообразования зависит от наследственных факторов и влияния внешних факторов. 2. Факультативные (необязательные) – патологические изменения ткани, не связанные с наследственными или врождёнными дефектами, на фоне которых может развиться злокачественное заболевание: хронические воспалительные заболевания и очаги пролиферации, вызванные гормональной перестройкой, рубцы после ожогов, незаживающие язвы, эрозии шейки матки, полипы, старческие кератозы. При этом, чем дольше существуют факультативные предопухолевые заболевания, тем выше вероятность развития злокачественного новообразования. Влияют Состояние ферментных, гормональной и иммунной систем организма влияют на возникновение и развитие злокачественного заболевания: 1. Аллергия – аллергизация организма отрицательно влияет на его устойчивость к возникновению злокачественного процесса. Однако при возникновении злокачественного новообразования состояние организма и прогноз лучше в тех случаях, когда организм способен к осуществлению аллергических реакций, чем тогда, когда он к этому не способен. Это несоответствие объясняется сохранением хотя бы в какой-то мере способности к иммунной реакции организма, обеспечивающей противоопухолевую защиту. 2. Иммунитет – снижение устойчивости макроорганизма к возникновению злокачественного заболевания при иммунной перестройке, сочетается со снижением клеточного и гуморального аутоиммунитета, взаимосвязанных иммунных механизмов противоопухолевой защиты. В онтогенезе иммунный ответ развивается неполноценно в старости, именно в этот период наиболее часто возникают злокачественные заболевания. 3. Воспаление – явления раздражения, повреждения и функциональной дезорганизации, имеющие место при воспалении и возникающие при этом аутоиммунные процессы, действующие в совокупности с другими факторами, благоприятствуют возникновению и развитию злокачественного процесса. 4. Метаболический синдром – комплекс метаболических, гормональных и клинических нарушений, являющихся факторами риска раннего развития атеросклероза и его сердечно-сосудистых осложнений. В основе патогенеза метаболического синдрома лежит первичная инсулинорезистентность и сопутствующая системная гиперинсулинемия. Метаболический синдром – совокупность трех и более хронических болезней: ожирение, артериальная гипертония, диабет, дислипидемия, повышенный уровень холестерина и др. Метаболический синдром способствует развитию воспалительных процессов в организме и повышает риск возникновения злокачественного новообразования. 5. Реактивность и соединительная ткань: соединительнотканные клеточные элементы (ретикулоэндотелиальная система, система макрофагов) участвуют в формировании реактивности организма. Они обладают фагоцитарной активностью, обеспечивают интенсивность заживления ран, обладают барьерной и антитоксической функцией. Угнетение высшей нервной деятельности сопровождается угнетением поглотительной функции элементов соединительной ткани, угнетением процессов заживления ран, воспаления и пр. Возбуждение высшей нервной деятельности стимулирует указанные функции соединительнотканных клеток. Факторы риска Анализ семи наиболее распространенных злокачественных заболеваний: легкого, молочной железы, желудка, толстой кишки, шейки и тела матки, предстательной железы показал, что в основе предопухолевых заболеваний лежат следующие факторы риска: – генетический или наследственный – возможен от 1 до 15% случаев, когда происходит передача «кровным» родственникам предрасположенности к возникновению и развитию злокачественного заболевания; – экзогенный – особенности питания, инфекция, канцерогенные воздействия (ионизирующее излучение, эндо- и экзоканцерогены, вирусы) приводят к грубым морфологическим изменениям тканей с последующим развитием хронического воспаления, возможным возникновением и развитием злокачественного заболевания; – эндогенный – увеличение возраста, наличие или развитие хронических эндокринных, гиперпластических и других заболеваний, которые могут самостоятельно спровоцировать хроническое воспаление тканей или способствовать переходу острого в хроническое воспаление с последующим возникновением и развитием злокачественного заболевания. Таким образом, к предопухолевым относят очень широкий круг заболеваний: неспецифические изменения тканей воспалительного, дистрофического и дисгормонального характера; доброкачественные опухоли; пороки развития; возрастные изменения и др. 2. ПРЕДОПУХОЛЕВЫЕ ИЗМЕНЕНИЯ МЕСТНЫХ ТКАНЕЙ Предопухолевые изменения местных тканей – это неспецифические патологические изменения, возникающие в результате приспособительных процессов. Однако это не стадия последовательной трансформации нормальной пролиферирующей соматической клетки в злокачественную, а только необходимая подготовка тканей для создания условий при которых генотипически измененная клетка может приобрести эпигенетические изменения и трансформироваться в злокачественную клетку. ХАРАКТЕРИСТИКА ТКАНЕЙ Ткань – система клеток и их неклеточных производных, специализированная на выполнении определенных частных функций. Ткани имеют специализированные и малодифференцированные (камбиальные) клетки, а также неклеточные структуры: симпласты, межклеточные вещества, кутикулярные образования и т.д. Эпителиальные ткани – это совокупность дифферонов полярно дифференцированных клеток, тесно расположенных в виде пласта на базальной мембране, на границе с внешней или внутренней средой, а также образующих большинство желёз организма (Рис. 1). Различают две группы эпителиальных тканей: 1. Поверхностные эпителии – пограничные ткани, располагающиеся на поверхности тела, слизистых оболочках внутренних органов и вторичных полостей тела: отделяют организм и его органы от окружающей их среды, участвуют в обмене веществ, предохраняют подлежащие ткани организма от различных внешних воздействий. 2. Железистый эпителий – осуществляет секреторную функцию: синтезирует и выделяет специфические продукты (секреты), которые используются в процессах, протекающих в организме.
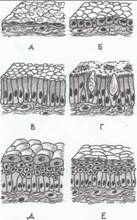
Рис. 1. Трехмерная система различных типов эпителия (А. Хэм, Д. Кормак, 1983, Т.2, стр. 9): А – однослойный плоский, Б – однослойный кубический, В-однослойный цилиндрический, Г – многорядный цилиндрический, Д – переходный, Е – многослойный плоский неороговевающий. Базальная мембрана – образуется в результате деятельности, как клеток эпителия, так и клеток подлежащей соединительной ткани (Рис. 2). Толщина ее может быть различной, очень тонка и плохо различима у кишечного эпителия. Функции базальной мембраны: 1. Механическая – закрепление эпителиоцитов. 2. Трофическая и барьерная – избирательный транспорт веществ. 3. Морфогенетическая – обеспечение процессов регенерации и ограничение возможности инвазивного роста эпителия.
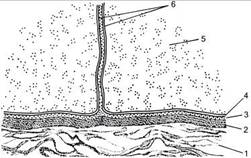
Рис. 2. Компоненты базальной мембраны (А. Хэм, Д. Кормак, 1983, Т.2, стр. 54): 1 – ретикулиновые волокна, 2 – базальная пластина, 3 – гликокаликс, 4 – плазматическая мембрана базальной клетки, 5 – цитоплазма, 6 – боковые мембраны смежных клеток.
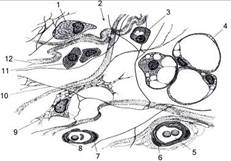
Рис. 3. Схематическое изображение рыхлой соединительной ткани (А. Хэм, Д. Кормак, 1983, Т.2, стр. 57): 1 – макрофаг, 2 – аморфное межклеточное вещество, 3 – плазматическая клетка, 4 – жировая клетка, 5 – кровеносный сосуд, 6 – гладкомышечная клетка, 7 – перицит и 8 – эндотелиальная клетка капилляра, 9 – фибробласт, 10 – эластическое волокно, 11 – тучная клетка, 12 – коллагеновое волокно. Соединительная ткань – является основным компонентом стромы любого органа или ткани (Рис. 3). Функционирует в норме и патологии на основе взаимовыгодного сотрудничества клеточных элементов между собой и с межклеточным матриксом и обратной связи с паренхимой и клетками крови, поэтому ее можно рассматривать, как саморегулирующуюся систему. Соединительные ткани – это полужидкая мукополисахаридно-белковая среда, в которой находятся: 1. Разнообразные клеточные элементы: лейкоциты, моноциты, макрофаги, фибробласты, тучные клетки, лимфоциты, плазматические клетки и др. 2. Волокнистые образования: коллагеновые, эластические и ретикулиновые волокна 3. Аморфное вещество – гелеобразная субстанция, в которую погружены волокна и клетки соединительной ткани, представляет собой метаболическую, интегративно-буферную многокомпонентную среду. В ее состав входят: вода, белки плазмы крови, неорганические ионы, продукты метаболизма паренхиматозных клеток, растворимые предшественники коллагена и эластина, протеогликаны, гликопротеины и комплексы, образованные ими. Соединительные ткани участвуют в поддержании гомеостаза внутренней среды и отличаются от других тканей меньшей потребностью в аэробных окислительных процессах. Функции соединительной ткани: трофическая, защитная, опорная (или биомеханическую), пластическая, морфогенетическая. ВОСПАЛЕНИЕ Kousmine C. (1956): раковый процесс – это своеобразная форма воспаления. Воспаление – это возникшая в ходе эволюции защитно-приспособительная реакция живых систем, проявляющаяся комплексом местных патологических процессов морфологического, функционального и физико-химического характера в ответ на воздействие разнообразных раздражителей. Известно, что злокачественный процесс никогда не возникает в здоровых тканях, этому предшествуют те или иные хронические патологические изменения местных тканей, которые называют «предопухолевыми». На одном из первых мест, среди хронических патологических изменений местных тканей, имеющих принципиальное научно-практическое значение, находится воспаление. Острое воспаление Острое воспаление – непосредственный и ранний ответ на повреждающий агент, складывается из трех основных компонентов: альтерации, расстройства микроциркуляции и пролиферации. 1. Альтерация – повреждение тканей: дегенеративные, деструктивные и некробиотические явления. Разрушение ткани вызывают ферменты лизосом клеток поврежденных в ходе воспалительного процесса: лейкоцитов, моноцитов, макрофагов, паренхиматозных клеток местных тканей. Следствием активации процессов протеолиза, гликолиза и липолиза является образование и освобождение большого количества органических кислот цикла Кребса, жирных кислот, молочной кислоты, полипептидов и аминокислот. Следствием этих процессов является увеличение осмотического давления – гиперосмия. Увеличение концентрации водородных ионов (Н+) приводит к гипероксии и ацидозу. Разрушение клеток сопровождается накоплением в воспаленной ткани ионов калия, натрия, хлора, анионов фосфорной кислоты и др. 2. Расстройства микроциркуляции: в ранние сроки начала воспаления возникают кратковременный спазм артериол, с последующим расширением капилляров, артериол и венул. Затем по мере нарастания воспалительного процесса – застой и стаз крово- и лимфообращения. При этом в воспаленную ткань из сосудистого русла выходят жидкая часть крови (экссудация) и форменные элементы: лейкоциты (нейтрофилы), моноциты и лимфоциты. Нейтрофилы в очаге воспаления помогают организму очистить зону повреждения от инфекции и продуктов распада аутологичных клеток, а Мононуклеары (моноциты, макрофаги и лимфоциты) контролируют программу репаративной регенерации. 3. Пролиферация – реакция размножения элементов соединительной ткани. Фибробласты митотически делятся, создавая колонии, и вместе с лейкоцитами образуют воспалительный инфильтрат. Кроме того, в периферической крови человека имеются полипотентные малодифференцированные клетки соединительнотканного ряда, именуемые, как «фиброциты периферической крови» или фибробластоподобные клетки, способные мигрировать в участки повреждения тканей и участвовать в процессе формирования как нормальных, так и патологических рубцов. Хроническое воспаление Под хроническим воспалением понимают продолжительный процесс (месяцы и годы), при котором повреждение тканей, реактивные изменения и рубцевание развиваются одновременно. Хроническое воспаление может следовать вслед за острым воспалительным ответом, который не приводит к уничтожению повреждающего агента или протекает без клинически видимой острой стадии. Причины хронического воспаления многообразны: – различные формы фагоцитарной недостаточности; – длительный стресс и другие состояния, сопровождающиеся повышенной концентрацией в крови катехоламинов и глюкокортикоидов; – повторное повреждение ткани или органа; – персистирующая инфекция и / или интоксикация; – патогенное действие факторов иммунной аутоагрессии. Патогенез хронического воспаления отличается от острого воспаления тем, что длится достаточно долго для того, чтобы возникли иммунный ответ и регенерация. Большинство агентов, приводящих к развитию хронического воспаления, вызывают прогрессивный и часто обширный некроз ткани, который сопровождается замещением фиброзной тканью. Выраженность фиброза в тканях зависит от продолжительности хронического воспаления. Хроническое воспаление может быть первичным и вторичным: – если воспаление изначально имеет вялое и длительное течение, его называют «первично-хроническим»; – если течение воспаления после острого периода приобретает затяжной характер, то оно обозначается как «вторично-хроническое». Для хронического воспаления характерен ряд признаков: гранулёмы, капсула, некроз, преобладание моноцитарного и лимфоцитарного инфильтрата. Учитывая наличие большого количества мононуклеарных фагоцитов и лимфоцитов, хроническое воспаление обозначают как мононуклеарно-инфильтративное, отражающее: персистирующую реакцию на повреждение, разрушение тканей, попытку восстановления разрушенных тканей путем их замещения соединительной тканью или фиброзом, новообразование мелких кровеносных сосудов (ангиогенез). Хроническое воспаление диагностируется благодаря его морфологическим особенностям. Оно отличается от острого воспаления отсутствием основных признаков: покраснения, припухлости, боли, повышения температуры. Активная гиперемия, экссудация жидкости и эмиграция нейтрофилов при хроническом воспалении не выражены. Исход воспаления Имеются несколько возможных исходов воспаления: – при не осложненном остром воспалении ткань возвращается к нормальной жизнедеятельности путем разжижения и удаления экссудата и клеточного детрита макрофагами и лимфатической системой; – если при остром воспалении резко выражен некроз ткани, то восстановление ее происходит путем регенерации или замещения соединительной тканью с формированием рубца; – если повреждающий агент не нейтрализуется при остром воспалительном ответе, развивается иммунный ответ, который приводит к развитию хронического воспаления; – если в результате хронического воспаления достигается удаление или нейтрализация повреждающего агента, ткань также регенерирует, обычно путем фиброза. В процессе пролиферации происходит рассасывание мелких тромбов и погибших тканей (ферментативное расщепление, фагоцитоз). Большие дефекты тканей, образующиеся в результате фибринозно-некротического воспаления, замещаются рубцовой тканью. Мелкие дефекты, возникающие между клетками внутри местных тканей (стромы) сначала становятся просветами, затем превращаются в микрополости. Впоследствии сформированные микрополости становятся «кладбищем» для погибших клеток, т. к. активный процесс альтерации и пролиферации не успевают быстро уничтожить и лиминировать слабые и поврежденные клетки местных тканей и клетки крови. Изменения межклеточного вещества Физико-химические изменения межклеточного вещества и ткани при воспалении значительны и выражаются в следующих нарушениях: – нарастает ацидоз – Н – гипериония; – увеличивается количество К и Na – ионов; – нарастает осмотическое давление; – нарастают ферментативно-аутокаталитические процессы; – увеличивается СО2 в тканях; – понижается поверхностное натяжение коллоидов протоплазмы (эритроцитов, лейкоцитов, гистиоцитов), что делает клетки более липкими, способствует феномену «краевого стояния» и влечет за собой изменения клеточной конфигурации. Воспалительный отек образуется вследствие повышения адсорбционных процессов, т.е. связывания воды, белков и солей тканями в результате нарастания в них осмотической концентрации, изменению вязкости вышедших белков и явлению свертывания их при соприкосновении с денатурированными тканевыми поверхностями. В основе связывания воды лежит эндосмотическая и молекулярная имбибиция структурных элементов с их разбуханием и гомогенизацией (аморфизацией), а также прекращением циркуляции в тканевых щелях. В то же время воспалительная реакция имеет и защитно-приспособительное значение для организма: белки отечной жидкости способны связывать и фиксировать бактериальные токсины, а также нейтрализовать токсические продукты распада тканей. Это задерживает поступление указанных выше веществ из очага воспаления в общую циркуляцию и предупреждает распространение их по организму. Таким образом, патологические изменения местных тканей при воспалении, могут быть представлены, как предопухолевые изменения тканей. 3. ФОРМИРОВАНИЕ ИЗОЛИРОВАННОЙ МИКРОПОЛОСТИ Зюсс Р. И др. (1977): процесс «зарождения» злокачественной клетки и развития злокачественного процесса, каким-то образом ускользают из-под контроля регуляции роста в организме-носителе. Это возможно лишь в том случае, если вышеуказанные процессы будут происходить в достаточно изолированном от самого организма-носителя пространстве, находящемся в его же тканях. Для «зарождения» стволовой злокачественной клетки, последующего роста и развития злокачественного процесса, необходимы условия создающие изолированное состояние клетки-предшественницы от влияния организма. Эти условия можно назвать, как «предопухолевое» ложе в патологически измененных местных тканях на фоне предопухолевых заболеваний макроорганизма. «Предопухолевым» ложем может быть изолированная микрополость, формирование которой при хроническом воспалении – естественный процесс. Однако совершенно не обязательно, что сформировавшаяся изолированная микрополость станет местом, где произойдет «зарождение» стволовой злокачественной клетки. В эпителиальной ткани возникновение изолированной микрополости невозможно, по причине отсутствия необходимых для этого соединительнотканных структур, краткосрочности жизни эпителиальных клеток, а также тесного соединения их между собой и базальной мембраной. Базальная мембрана играет очень важную роль в образовании изолированной микрополости, т. к. является надежным барьером охраняющим «предопухолевое» ложе от внешних воздействий. Соединительная ткань является идеальным местом для формирования «предопухолевого» ложа, т. к. основные ее составляющие: клеточные диффероны, волокнистые структуры и аморфное вещество, при определенной организации могут участвовать в формировании изолированной микрополости. ПРОТОТИП Прототипом формирования изолированной микрополости, как «предопухолевого» ложа, может быть структурная организация желточного мешка зародыша человека (Рис. 4). Желточный мешок или пузырь (Vesicula umbilicalis) зародыша человека – это мешкообразный придаток на брюшной стороне зародыша, не имеющий в себе запаса питательного желтка. Стенка желточного мешка состоит из одного зародышевого листка, полость его наполнена жидкостью, содержащей белок, и соединена с полостью кишечника желточным протоком. Желточный мешок является вспомогательной структурой, обеспечивающей в первом триместре беременности питание и кроветворение эмбриона. На протяжении своего существования желточный мешок может расти до 2 – 6 мм в диаметре. После 8 – 9 недель беременности его значение в развитии эмбриона начинает уменьшаться и к концу первого триместра он полностью редуцируется.
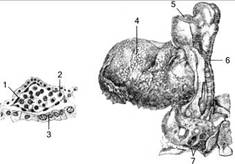
А Б Рис. 4. Развитие кровяных островков в желточном мешке у зародыша человека (Carnegie Cont. To Emb., 1929, vol.20): А – начало дифференцировки эндотелия и первичных клеток крови у 4-недельного зародыша (длина зародыша 4,5 мм): 1 – первичные кровяные клетки, 2 – клетки крови, 3 – эндодерма. Б – зародыш на стадии 10 сомитов по Корнеру: 4 – примордиальный кровяной островок в желточном мешке, 5 – сердечный выступ, 6 – срезанный край амниона, 7 – пупочные сосуды. Принцип построения и функционирования желточного мешка, как нельзя лучше является прототипом построения и функционирования изолированной микрополости, как будущего «предопухолевого» ложа, при этом: 1. Внутри микрополости возникают условия, близкие к эмбриональным. 2. «Зарождение» и размножение стволовой злокачественной клетки изначально происходит в замкнутой изолированной от микроокружения системе. 3. Стволовая злокачественная клетка условно повторяет начало эмбрионального кроветворения. 4. Имеется некоторое количество питательных веществ. 5. Создается агрессивная бескислородная среда. УСЛОВИЯ 1. Врожденное и / или приобретенное формирование патологических полостей и фиброзных перегородок, рубцов, капсул вокруг инородного тела, приводит к нарушению микроциркуляции внеклеточной жидкости и способствует возникновению и развитию вялотекущих хронических воспалительных явлений с возможным формированием изолированной микрополости. 2. Разрушение тканей (альтерация) способствует возникновению просветов в межклеточном пространстве, способных превратиться в микрополость. 3. Наличие отека местных тканей при воспалении сопровождается скоплением жидкости (экссудата) в отдельных местах – в просветах, некоторые из них при накоплении экссудата могут превратиться в микрополость. 4. В процессе воспаления возникают значительные химические изменения межклеточной жидкости, которая может скапливаться в естественно формирующейся микрополости, превращая ее в объемное образование, содержащее агрессивную специфическую жидкость. 5. Регенеративный процесс (пролиферация), создает возможности для образования грануляционной и / или рубцовой ткани, которые могут развиваться вокруг образовавшейся микрополости, превращая ее в изолированное состояние с низким содержанием кислорода или его отсутствием. 6. Наличие в организме человека полипотентных малодифференцированных клеток соединительнотканного ряда периферической крови, именуемых, как «фиброциты периферической крови» или фибробластоподобные клетки, способных мигрировать в участки повреждения тканей и участвовать в процессе формирования как нормальных, так и патологических рубцов, а также изолированной микрополости. МЕХАНИЗМ Вирхов Р. (1863–1867): хроническое раздражение тканей вызывает с их стороны защитную реакцию – идет регенерация и скорость деления клеток увеличивается, но если будет утерян контроль за регенерацией и скоростью деления, то могут возникать злокачественные клетки. Хроническое воспаление возникает на фоне продолжающегося острого воспаления, причем регенеративные и воспалительные процессы могут долго существовать параллельно, ослабевая и усиливаясь один за счет другого. При этом в соединительной ткани из-за локальных неоднородностей распределения веществ и нарушения передвижения жидкости происходит его накопление в ограниченных зонах межклеточного пространства. Известно, что первоначально в зону воспаления приходят нейтрофилы, которые в очаге воспаления помогают организму очистить зону повреждения от инфекции и продуктов распада аутологичных клеток, подготавливая тем самым «фронт работы» для Моноцитов-Макрофагов. В решении этой задачи нейтрофилы порой «усердствуют» вызывая «взрыв» разрушений местных тканей. Именно нейтрофилы обеспечивают образование микрополости, т. к. они вызывают деструкцию соединительнотканного матрикса, образуют экссудат и привлекают клетки, обеспечивающие репарацию. В процессе воспаления происходит рассасывание мелких тромбов и погибших тканей. Большие дефекты тканей, образующиеся в результате фибринозно-некротического воспаления, замещаются рубцовой тканью. Мелкие дефекты, возникающие между клетками внутри стромы, сначала становятся просветами, затем превращаются в микрополости. В ответ на повреждение тканей и под действием патогенетических факторов воспаления, из кровеносного русла мигрируют полипотентные малодифференцированные клетки соединительнотканного ряда, именуемые, как «фиброциты периферической крови» или фибробластоподобные клетки. Их иммунофенотипические признаки в сочетании со способностью давать начало представителям фибропластического клеточного дифферона, позволяют утверждать, что они представляют собой мультипотентные мезенхимальные стромальные клетки (ММСК), постоянно циркулирующие в крови в небольших количествах. Именно эти фибробластоподобные клетки и участвуют в формировании изолирующей оболочки микрополости Завершающим этапом является возникновение инфильтрата, состоящего из мелких лимфоидных клеток являющихся, главным образом, продуктом размножения местных соединительнотканных элементов. Цементирующим веществом, покрывающим денатурированные поверхности импровизированной оболочки организовавшейся микрополости, является фибрин – полимеризованный продукт белка крови фибриногена. Необходимо отметить, что процесс хронического воспаления – длительный и затяжной, может протекать месяцы и годы, значит и длительность формирования изолированной микрополости, также может составлять месяцы и годы. СТРОЕНИЕ Микрополость окружена несколькими слоями, образующими оболочку. Каждый из слоев может быть различно выраженным и каждый из них выполняет свою роль: 1. Внутренний – малые пролиферирующие фибробласты, не образующие сплошного монослоя, лежащие на среднем слое. Синтезируют компоненты межклеточного вещества белков (коллаген, эластин), протеогликанов, гликопротеинов, тем самым способствуют формированию соединительнотканной оболочки, также выступают в качестве подложки-фидера (от англ. feed – кормление, питание). Laki (1974): пролиферация фибробластов идет на фибринных сгустках, как при заживлении ран, где фибрин играет роль матрицы, необходимой для регенерации тканевой структуры. Герасимов И.Г., Попандопуло А.Г. (2007): фибробласты, распластанные в монослое, в результате лишения их CO2 в концентрации, необходимой для нормального функционирования, утрачивают контакт друг с другом, округляются и погибают путем некроза или апоптоза. 2. Средний слой – в основном это коллагеновые волокна, которые окружают микрополость достаточно плотным кольцом и, тем самым, изолируют микрополость от влияния микроокружения. 3. Наружный слой – не постоянный, различный по объему инфильтрат, состоящий по преимуществу из мелких лимфоидных клеток являющихся, главным образом, продуктом размножения местных соединительнотканных элементов. 4. O, Meara (1958): обнаружил фибриновые волокна в гистологических препаратах опухолей. Фибрин возникает в результате повышения проницаемости сосудистой стенки, выхода белков плазмы крови в межклеточное пространство и явлению свертывания фибриногена. Свойства фибрина: – является цементирующим материалом при соприкосновении с денатурированными тканевыми поверхностями окружающими сформированную микрополость; – влияет на рост опухоли, т. к. может служить источником питания злокачественных клеток; – защищает злокачественные клетки от разрушающего действия со стороны организма-носителя и тем самым содействует злокачественному росту; – препятствует отрыву злокачественных клеток от основной массы опухоли; – стимулирует активность процессов приживления разрозненных злокачественных клеток, дающих начало новым злокачественным очагам. ФОРМА И ЛОКАЛИЗАЦИЯ Изолированная микрополость равномерно заполнена жидкостью и имеет различную форму: щелевидную, овальную, округлую, звездчатую и др. (Рис. 5).
Рис. 5. Изолированная микрополость Размеры микрополости зависят: – от длительности и характера течения хронического воспаления; – количества находящейся в ней жидкости; – морфологического строения органа или ткани, в котором расположена микрополость; – способности организма-носителя отграничить микрополость. Первично сформированная изолированная микрополость имеет размеры до 1 мм, в дальнейшем ее размеры могут увеличиваться по мере увеличения массы злокачественных клеток за счет экспансивного роста. Локализация и глубина залегания изолированной микрополости зависит от многих причин, одна из них – это рельеф слизистой оболочки: – если рельеф слизистой оболочки «плоский» (протоки молочной железы, протоки предстательной железы, шейка матки и др.), то микрополость может формироваться под базальной мембраной, возможно участие базальной мембраны в формировании ее оболочки; – если рельеф слизистой оболочки «сложный» (желудок, толстая кишка, легкие и др.), то микрополость формируется в глубине соединительной ткани, на уровне экзокринных желез. ХИМИЧЕСКИЙ СОСТАВ ЖИДКОСТИ Физико-химические изменения межклеточного вещества в зоне хронического воспаления значительны и выражаются в нарушении нормальной установки коллоидных систем: – увеличивается осмотическое давление (гиперосмия) – аналогично и в изолированной микрополости; – увеличивается концентрация водородных ионов (гипероксия и ацидоз) – аналогично и в изолированной микрополости; – ионы калия, натрия, хлора, анионы фосфорной кислоты и др. накапливаются вследствие разрушения клеток – все они или каждый в отдельности могут находиться в изолированной микрополости; – белки отечной жидкости, а также белки связанные с бактериальными токсинами и токсическими продуктами распада тканей – могут находиться в изолированной микрополости; – ферменты лизосом (протеазы, катепсин, химотрипсин, щелочная фосфатаза и др.) клеток поврежденных в ходе воспалительного процесса скапливаются в большом количестве в межклеточной жидкости – могут находиться в изолированной микрополости; – белки–медиаторы воспаления с ферментативными свойствами (например, некрозин) – могут находиться в изолированной микрополости; – органические кислоты цикла Кребса, жирные кислоты, молочная кислота, полипептиды и аминокислоты, возникшие в большом количестве вследствие активации процессов протеолиза, гликолиза и липолиза – все они вместе или каждая в отдельности могут находиться в изолированной микрополости; – кислород количественно уменьшается, а увеличивается содержание углекислого газа в тканях, в изолированной микрополости создается бескислородная среда. Таким образом, в зоне хронического воспаления формируется «предопухолевое» ложе в виде изолированной микрополости, внутри которой возникает среда характеризующаяся, как «суперусловия». 5. Инициация костномозгового мононуклеара Костный мозг является одновременно органом кроветворения и центральным органом иммунной системы. Общая масса костного мозга у взрослого человека примерно 2,5–3,0 кг (4,5–4,7% от массы тела). Около половины составляет красный костный мозг, располагающийся в ячейках губчатого вещества плоских и коротких костей, эпифизов длинных (трубчатых) костей. Остальное – желтый костный мозг, выполняющий костномозговые полости диафизов длинных (трубчатых) костей. В состав костного мозга входят стволовые клетки, из которых формируются основные клеточные элементы крови, клеточные элементы скелетных тканей, клеточные элементы сосудов. Чем моложе человек, тем активнее стволовые клетки костного мозга. 1. ГЕМОПОЭЗ Гемопоэз (от греч. háima – кровь и póiēsis – сотворение) или кроветворение – процесс образования, развития и созревания клеток крови у животных и человека. Все клетки крови происходят из единой родоначальной клетки – полипотентной стволовой кроветворной клетки в эмбриогенезе и после рождения, они обладают способностью к дифференцировке во все без исключения клетки крови и возможностью участия в образовании других тканей организма. Различают эмбриональный и постэмбриональный гемопоэз. ЭМБРИОНАЛЬНЫЙ Эмбриональный гемопоэз представляет собой процесс развития крови, как ткани в эмбриональном периоде развития человека в результате последовательно сменяющихся трех основных этапов: 1. Первый этап – мезобластический: у человека начинается в конце 2-й – в начале 3-й недели, протекает по 9-ю неделю развития зародыша и характеризуется появлением первой генерации стволовых клеток крови. При этом клетки крови появляются во внезародышевых органах: мезенхиме стенки желточного мешка, мезенхиме хориона и стебля. Кроветворение в стенке желточного мешка: в мезенхиме обособляются зачатки сосудистой крови или кровяные островки. В них клетки округляются, теряют отростки и преобразуются в стволовые клетки крови. Клетки, ограничивающие кровяные островки, уплощаются, соединяются между собой и образуют эндотелиальную выстилку будущего сосуда. Часть стволовых клеток дифференцируется в первичные клетки крови (бласты). В поддержании плюрипотентности эмбриональных стволовых клеток млекопитающих, большое значение играют фибробласты в качестве подложки-фидера (от англ. feed – кормление, питание). 2. Второй этап – гепатолиенальный: начинается с 5–6-й недели развития плода, когда печень становится основным органом гемопоэза, в ней образуется вторая генерация стволовых клеток крови. Кроветворение в печени достигает максимума через 5 месяцев и завершается перед рождением. Стволовые клетки крови печени заселяют тимус, селезенку и лимфатические узлы. 3. Третий этап – медуллярный (костномозговой): начинается с 10-й недели и постепенно нарастает к рождению, характеризуется появлением третьей генерации стволовых клеток крови в красном костном мозге. После рождения красный костный мозг становится центральным органом гемопоэза. Необходимо отметить, что все органы, в которых осуществляется кроветворение: лимфатические узлы, печень, селезенка, вилочковая железа и костный мозг, обладают определенными анатомо-физиологическими особенностями и имеют общие черты строения: – строму составляет ретикулярная ткань, паренхиму – кроветворные клетки; – богаты элементами, относящимися к системе Мононуклеарных фагоцитов; – имеют капилляры синусоидного типа. ПОСТЭМБРИОНАЛЬНЫЙ Постэмбриональный гемопоэз представляет собой процесс физиологической регенерации крови, компенсирующий физиологическое разрушение дифференцированных клеток. Нормальное кроветворение осуществляется одновременно многими клонами – поликлонально и все клетки крови имеют костномозговое происхождение. Структура костного мозга Костный мозг обладает определенными анатомо-физиологическими особенностями. Его строму составляет ретикулярная ткань, паренхиму – кроветворные клетки. У человека красный костный мозг является высоко васкуляризированным органом, сообщается с кровотоком посредством капиллярной сети. Различают два типа капилляров: питающие (обычные) и функциональные (синусоиды), которые впадают в общий ствол – центральную вену. Синусоиды располагаются радиарно, между ними находится гемопоэтическая ткань. В синусах между эндотелиальными клетками имеются поры, связывающие ткань кроветворных органов с кровеносным руслом. Такое строение обеспечивает транспорт клеток в кровь, а также поступление из крови в кроветворные органы гуморальных факторов (гемопоэтинов), которые наряду с нервной системой оказывают влияние на кроветворение. Будучи гистогенетически единой, кроветворная система в своем функционировании характеризуется определенной независимостью поведения отдельных ростков кроветворения. Интенсивность гемопоэза Владимирская Е.Б. (2001): у мужчин массой тела 70 кг, в сутки образуется 1 х 10 в 11 степени лейкоцитов и 2 х 10 в 11 степени эритроцитов, что составляет клеточную массу в 300 грамм (100 + 200 грамм соответственно) в сутки, в месяц образуется 9 кг клеток, в год – около 100 кг. За 70 лет жизни клеточная продукция нормального кроветворения очень велика и составляет порядка 7 тонн клеток крови. Кроветворение в красном костном мозге Кроветворение в красном костном мозге происходит островками, в которых группируются клетки по росткам гемопоэза. Предшественники и развивающиеся кроветворные клетки расположены следующим образом: в центре – делящиеся и незрелые клетки, на периферии (около стенок синусоидов) – более зрелые клетки. Из полипотентной стволовой кроветворной клетки в красном костном мозге формируются все форменные элементы крови, развитие которых происходит экстраваскулярно. Часть их сохраняется в костном мозге в недифференцированном состоянии. Они могут расселяться по другим органам и тканям и являться источником развития клеток крови и соединительной ткани. Полипотентные стволовые кроветворные клетки относятся к самоподдерживающейся популяции клеток, и они редко делятся.
Рис. 6. Обобщенная схема первых трех классов кроветворения: 1 класс – полипотентная стволовая кроветворная клетка. П класс – полипотентные клетки-предшественницы лимфоцито- и миелопоэза. Ш класс – унипотентные клетки-предшественницы Т и В-лимфоцитов; би- и унипотентные клетки-предшественницы гранулоцитарного, эритроцитарного, моноцитарного и мегакариоцитарного гемопоэза. Все стадии костномозгового кроветворения составляют шесть основных классов: I класс – полипотентная стволовая кроветворная клетка – общая родоначальная клетка. Каждая полипотентная стволовая кроветворная клетка образует одну колонию и называется колониеобразующей единицей (КОЕ). Исследование клеточного состава колоний позволило выявить две линии их дифференцировки. II класс – одна линия дает начало полипотентной клетке-предшественнице – родоначальнице гранулоцитарного, эритроцитарного, моноцитарного и мегакариоцитарного ростка гемопоэза – родоначальнице миелопоэза (КОЕ-ГЭММег). Вторая линия дает начало полипотентной клетке-предшественнице – родоначальнице лимфоцитопоэза (КОЕ-Л). III класс – из полипотентных клеток дифференцируются би- и унипотентные родоначальные клетки. Методом колониеобразования определены би- и унипотентные клетки-предшественницы родоначальницы моноцитов (КОЕ-М), гранулоцитов и моноцитов (КОЕ-ГМ), нейтрофильных гранулоцитов (КОЕ-Гн), эозинофилов (КОЕ-Эо), базофилов (КОЕ-Базо), эритроцитов (БОЕ-Э и КОЕ-Э), мегакариоцитов (КОЕ-Мег), мегакариоцитов и эритроцитов (КОЕ-МегЭ). И унипотентные родоначальные клетки-предшественницы для Т- и В-лимфоцитов. IV класс – из би- и унипотентных родоначальных клеток-предшественниц образуются бластные клетки различных линий гемопоэза, идентифицируемые при анализе миелограммы (эритробласт, мегакариобласт и т.д.); V класс – созревающие клетки различных линий гемопоэза. VI класс – зрелые клетки различных линий гемопоэза. Все клеточные элементы, входящие в первые 3 класса и онтогенетически связанные, морфологически – не дифференцируемы (Рис. 6). Если даже обращается внимание на особенности в структуре ядра и цитоплазмы, то при изучении гематологических препаратов, их относят к лимфоидным элементам и бластным клеткам. Морфологически распознаваемые – это клетки 1У, У и У1 классов. В процессе дифференцировки морфологически распознаваемые клетки эритроцитарного ряда претерпевают 5–6 митозов, гранулоцитарные клетки – 4 митоза, при моноцитопоэзе от монобласта до макрофага происходит 7–8 митозов. Образующиеся в красном костном мозге клетки по мере созревания равномерно поступают в кровеносное русло, при этом время циркуляции их постоянно: эритроциты 100–120 суток и погибают, тромбоциты около 7–10 суток и погибают, нейтрофилы менее 6–8 часов и погибают, моноциты 1,5–4,5 суток и выходят в ткани. МИКРООКРУЖЕНИЕ Миелоидная и лимфоидная ткани относятся к тканям внутренней среды и являются разновидностями соединительной ткани. В них представлены две основные клеточные линии – клетки ретикулярной ткани и гемопоэтические клетки, т.е. для них характерно наличие стромальных и гемопоэтических элементов, образующих единое функциональное целое. Ретикулярные, а также жировые, тучные и остеогенные клетки вместе с межклеточным веществом формируют микроокружение для гемопоэтических элементов. Структуры микроокружения и гемопоэтические клетки функционируют в неразрывной связи друг с другом. Микроокружение оказывает воздействие на дифференцировку клеток крови при контакте с их рецепторами или путем выделения специфических факторов. РЕГУЛЯЦИЯ Стволовые кроветворные клетки в стадии созревания находятся под строгим регулирующим контролем, механизм которого достаточно не изучен. В регуляции процессов пролиферации и дифференцировки гемопоэтических клеток большую роль играют: 1. Стромальное микроокружение: – клеточный компонент: фибробласты, жировые клетки, макрофаги, остеобласты, эндотелиальные клетки; – внеклеточный (экстрацеллюлярный) матрикс, который составляют продукты секреции стромальные клеток: коллаген, фибронектин, ламинин, гликозаминогликаны и другие белковые компоненты. 2. Факторы роста – обеспечивают пролиферацию и дифференцировку стволовых кроветворных клеток, и последующие стадии их развития. Факторы роста включают: – колониестимулирующие факторы (КСФ) – стимулируют гемопоэз. Среди них наиболее изучены факторы, стимулирующие развитие гранулоцитов и макрофагов (ГМ-КСФ, Г-КСФ, М-КСФ); – ингибирующие факторы – тормозят гемопоэз. Выделен ингибирующий лейкемию фактор (ЛИФ), который тормозит пролиферацию и дифференцировку моноцитов-макрофагов; – интерлейкины. 3. Факторы транскрипции – влияют на экспрессию генов, определяют направление дифференцировки гемопоэтических клеток (поэтины). 4. Витамин В12 – необходим для стимуляции пролиферации и дифференцировки гемопоэтических клеток. Таким образом, кроветворение в красном костном мозге – это единственная локализация ткани в организме человека, где в эмбриональном и постэмбриональном периодах жизни сконцентрировано большое количество клеток различной потентности и происходит интенсивная пролиферация. 2. МОНОНУКЛЕАРНАЯ ФРАКЦИЯ В СИСТЕМЕ КРОВИ Мононуклеарная фракция в системе крови – это клетки, выделенные из костного мозга или периферической крови посредством отделения от эритроцитов, тромбоцитов и гранулоцитов на градиенте плотности. МОНОЦИТОПОЭЗ Моноцитопоэз берет свое начала от полипотентной клетки-предшественницы родоначальницы миелопоэзе с последующим развитием в Моноцитарный росток (П класс), продолжается в унипотентную клетку-предшественницу родоначальницу Моноцитов (Ш класс). Однако клеточные элементы, входящие во П и Ш классы морфологически не дифференцируемы. Морфологическое распознавание начинается с бластной клетки Моноцитарного ростка (1У класс) – монобласт, который через стадию Промоноцит, превращается в Моноцит. В отличие от клеток других линий, цикл созревания которых заканчивается в красном костном мозге, клетки Моноцитарного ростка окончательно созревают только в тканях, где Промоноцит и Моноцит трансформируются в Макрофаг. Морфология клеток:По мере дифференцировки монобласта в промоноцит и моноцит клетка претерпевает ряд морфологических и функциональных изменений (Рис. 7): В красном костном мозге 1. Монобласт – диаметром 12–20 мкм. В норме его трудно отличить от миелобласта или недифференцируемого бласта, а также не всегда можно отличить от лимфобласта. Только отмеченные очертания ядра и более широкая светло-базофильная цитоплазма могут указать на развитие этого «бласта» в сторону моноцитарной клетки. Ядро нежной структуры содержит 1–2 нуклеолы голубоватого цвета. Цитоплазма голубого цвета, в ней могут присутствовать пылевидные азурофильные гранулы.
Рис. 7. Моноцитарный ряд клеток: А – монобласты, Б – промоноциты, В-моноциты. 2. Промоноцит – диаметром 15–20 мкм. В норме имеет ядро промиелоцита бобовидной формы, светло-фиолетового цвета. Хроматин нежный, крупносетчатый. В ядре 1–2 нуклеолы. Цитоплазма серо-голубого, дымчатого цвета с мелкой азурофильной зернистостью. Промоноцит, являясь клеткой-предшественницей Моноцита, проходит 2 последовательных цикла деления до превращения в Моноцит, продолжительность митотического цикла составляет 30 часов. Промоноцит способен к пиноцитозу и фагоцитозу, хотя в меньшей степени, чем Моноцит и Макрофаг. 3. Моноцит – диаметром 16–18 мкм, различных морфологических вариаций по характеру и интенсивности окраски ядра и цитоплазмы. Ядра могут приближаться к округлым, бобовидным формам. Моноцит с более нежной структурой ядра и наличием ядрышек (или их остатков) можно отнести к Промоноциту. Цитоплазма сероватого или бледно-голубого цвета, в ней могут присутствовать многочисленные пылевидные азурофильные гранулы. Дифференцировка Монобласта в Моноцит происходит в красном костном мозге в течение 5 дней. Моноцит в костном мозге находится в среднем 3 суток (минимальное время пребывания 9 часов), затем делится и, не образуя костномозгового резерва, выходит в периферическую кровь. В крови Моноцит – наиболее крупная клетка крови, здесь он созревает, ядро становится из круглого сначала бобовидным, затем лапчатым, меняется структура хроматина. В периферической крови обнаружен различный уровень дифференцировки Моноцитов, причем у здоровых людей преобладают более зрелые Моноциты. В незрелом Моноците есть остатки нуклеол, меняются ферменты в цитоплазме. В крови Моноциты распределяются на пристеночные и циркулирующие пулы, обменивающиеся между собой, количественные соотношения которых могут меняться. У человека циркулирующий пул Моноцитов в норме 18х10 в 6 степени клеток/кг массы тела, а маргинальный пул, который в данный момент не принимает участия в циркуляции, примыкая к внутренней стенке микрососуда, в 3,5 раза больше (63х10 в 6 степени клеток/кг). В целом общий пул Моноцитов периферической крови составляют от 1 до 10% всех лейкоцитов (80–600 х 10 9/л). Моноциты циркулируют в крови от 36 до 104 часов (1,5 – 4.5 суток) и затем покидают ее по стохастическому (целевому) принципу, взаимодействуя со специализированными адгезивными молекулами на эндотелиальных клетках. Миграция Мононуклеара из сосудистого русла в очаг воспаления происходит через участки микроциркуляторного русла с эндотелием второго типа – это посткапилляры и венулы. В ткани Van Furth R. (1988): после попадания в ткань Мононуклеары крови превращаются в Макрофаги, которые в свою очередь адаптируются к микросреде их будущего обитания. Разнородность популяции Макрофагов «по горизонтали» – микросреда, в которой они функционируют. Выйдя из кровеносного русла, Моноцит становится тканевым и больше не способен вернуться в циркуляцию. Тканевой Моноцит трансформируется в органо- и тканеспецифический Макрофаг согласно следующими стадиям перехода: макрофагальный бласт, промакрофаг, макрофаг. Макрофаг может образоваться из стволовой кроветворной клетки и из Промоноцита согласно тем же стадиям перехода. 4. Макрофаг (от греч. makros – большой, fagos – пожирающий) – гетерогенная специализированная клеточная популяция защитной системы организма (Рис. 8). Диаметром 15–80 мкм, форма клетки неправильная, ядро овальной или продолговатой формы. Продолжительность жизни исчисляется месяцами и годами. Возможно образование Макрофагов: в соединительной ткани (гистиоциты), легких (альвеолярные), печени (купферовские клетки), селезенке, лимфатических узлах, костной ткани (остекласты), нервной ткани (микроглиальные клетки), коже (клетки Лангерганса), в плевральном выпоте и асците и т.д. Макрофаги принимают активное участие: в неспецифической защите от патогенных микроорганизмов; в процессах репарации; инициации специфического иммунного ответа; в метаболизме липидов и железа; регуляции кроветворения; гемостазе; в секреции цитокинов и других биологически активных веществ, регулирующих пролиферацию, дифференцировку и функциональную активность различных клеток. По разнообразию фенотипических признаков Макрофагов можно судить о возможностях при трансформации Промоноцита и Моноцита и влиянии микроокружения. Макрофаг в сравнении с Промоноцитом и Моноцитом, по своим функциональным возможностям значительно превалирует. Значит, в процессе трансформации Макрофаг приобретает возможности, которые отсутствовали у Промоноцита и Моноцита.
Рис. 8. Макрофаги Промоноциты, Моноциты и Макрофаги человека в патологических условиях, способны к пролиферации в ограниченных масштабах. Промоноцит из этого ряда наиболее пролиферирующая клетка и может, минуя стадию Моноцита, в тканях трансформироваться в Макрофаг. СТИМУЛЯЦИЯ Учитывая, что Мононуклеары относятся к иммунокомпетентной системе, вполне законно ожидать изменение их количественного и качественного состояния при различных патологических процессах. В частности это наглядно проявляется при хроническом воспалении, когда число Моноцитов увеличивается. Это увеличение отмечается в красном костном мозге, периферической крови, селезенке, лимфатических узлах, перитонеальных полостях. При этом в периферической крови обнаружен различный уровень дифференцировки Моноцитов, а также могут появляться и преобладать менее зрелые клетки – Промоноциты. В ускоренном вариант пролиферации костномозговых Мононуклеаров получается: минимум 9 часов в красном костном мозге и 12 часов в кровеносном русле, итого 21 час. Для созревания Моноцита из Промоноцита необходимо два деления по 30 часов, т.е. при срочной потребности в Макрофагах, с учетом отсутствия костномозгового резерва, в кровеносное русло выходят Промоноциты и не зрелые Моноциты. В процессе дифференцировки морфологически распознаваемые клетки при Моноцитопоэзе претерпевают от Монобласта до Макрофага 7–8 митозов. При воспалительных процессах количество Макрофагов и их активность особенно возрастают. Воспалительный инфильтрат может поддерживаться лишь в случае постоянного обновления Мононуклеарных фагоцитов в очаге за счет Моноцитов крови. В свою очередь пул Моноцитов восстанавливается из красного костного мозга. Следовательно, через Мононуклеарные фагоциты очаг хронического воспаления приобретает постоянные связи с костным мозгом, с центром генерации свежих Моноцитов. Очаг будет прогрессировать при избыточном Моноцитопоэзе и наоборот. В то же время в стимуляции Моноцитопоэза самое деятельное участие принимают активированные Макрофаги. Таким образом, Промоноцит и Моноцит в системе кроветворения являются единственными промежуточными упрощенными универсальными клетками, которые в органах и тканях трансформируются в органо- и тканеспецифические Макрофаги. 3. МОНОНУКЛЕАР – КЛЕТКА-ПРЕДШЕСТВЕННИЦА ЗЛОКАЧЕСТВЕННОЙ КЛЕТКИ Клетка-предшественница – клетка, находящаяся на низком уровне дифференцировки, но уже коммитированная к развитию в клетки определенной линии. Аксиомой современной теории онкогенеза является положение, что клеткой-предшественницей стволовой злокачественной клетки является нормальная пролиферирующая соматическая клетка. Однако какая соматическая клетка явилась клеткой-предшественницей для злокачественной клетки, данной конкретной солидной опухоли – не известно. Достоверно доказаны очень важные и никем неоспоримые утверждения: – злокачественные клетки имеют больше сходства между собой, чем нормальные клетки между собой; – злокачественные клетки имеют меньше различий между собой, чем различия между злокачественными клетками и нормальными клетками; – нормальные клетки имеют меньше различий между собой, чем различия между нормальными клетками и злокачественными клетками; – основные принципы «зарождения» стволовой злокачественной клетки, роста злокачественного очага и развития злокачественного процесса различных органов и тканей совершенно идентичны. На этом основании можно говорить о злокачественных клетках, как об отдельной группе клеток, имеющих общее происхождение, а в совокупности со стромой, даже как об отдельной ткани в организме-носителе. В таком случае должна быть конкретная клетка, претендующая на роль «общего начала» или клетки-предшественницы первичной стволовой злокачественной клетки солидных опухолей. При анализе всех клеток организма человека необходимо выбрать, прежде всего, те клетки, которые имеют следующие основные свойства: 1. Являются соматическими пролиферирующими клетками с продолжительным жизненным циклом (месяцы, годы). 2. Обладают автономностью: умеют свободно перемещаться по всему организму-носителю, проникать и мигрировать в органах и тканях. 3. Способны влиять на различные жизненно важные процессы: гемопоэз, гомеостаз, иммунитет, пролиферацию, созревание и дифференцировку клеток и др. Клетками, обладающими вышеуказанными свойствами, в организме человека являются только клетки крови, из них: – эритроциты, тромбоциты и лейкоциты – это тупиковый вариант с коротким сроком жизни (эритроциты 100–120 суток, тромбоциты около 7–10 суток, нейтрофилы менее 6–8 часов), к тому же, имеют специфические черты и достаточно ограниченные функции, поэтому не могут претендовать на роль «общего начала»; – лимфоциты – относятся к Мононуклеарной фракции системы крови, имеют тропность к лимфоидной ткани и, как известно, унипотентные и полипотентные стволовые клетки лимфоцитопоэза являются клетками-предшественниками стволовых злокачественных клеток гемобластозов. Зрелые лимфоциты при воздействии на них специфических антигенов вновь способны трансформироваться в бластные клетки. Можно сказать однозначно, что лимфоциты прямо или косвенно участвуют в «зарождении» первичной стволовой злокачественной клетки, а также росте и развитии злокачественного процесса; – моноциты – относятся к Мононуклеарной фракции системы крови – прослеживают свое начало от полипотентной клетки-предшественницы родоначальнице миелопоэза с последующим развитием в Моноцитарный росток (П класс), который включает в себя достаточно большое количество клеток различной потентности (полипотентные, унипотентные) и местоположения (костный мозг, сосудистое русло, ткани). Поэтому все клетки, относящиеся к Моноцитарному ростку удобнее называть Мононуклеарная фракция или Мононуклеары. С учетом особенностей Мононуклеар является наиболее вероятным кандидатом на роль «общего начала» или клетки-предшественницы первичной стволовой злокачественной клетки солидных опухолей. Характеристика и возможности Мононуклеаров (Моноцитарный росток): 1. Морфологически недифференцируемые и дифференцируемые Мононуклеары подразделяются на три основные группы: – костномозговые: полипотентная клетка-предшественница родоначальница миелопоэза с последующим развитием в Моноцитарный росток, унипотентная клетка-предшественница родоначальница Моноцитов, монобласт, промоноцит, моноцит; – периферической крови: промоноцит, моноцит; – тканевые: промоноцит, моноцит, макрофагальный бласт, промакрофаг, макрофаг. Промоноцит и Моноцит присутствуют во всех трех группах клеток и являются промежуточным вариантом развития от костномозговой полипотентной клетки-предшественницы родоначальнице миелопоэза с последующим развитием в Моноцитарный росток (П класс) до органо- и тканеспецифического Макрофага, как конечного варианта развития. 2. Кроветворение в красном костном мозге, это единственный функционирующий очаг интенсивной пролиферации, который сохранился с эмбрионального периода развития и функционирует у взрослого человека. 3. Мононуклеары являются представителями клеток иммунокомпетентной системы и одновременно играют решающую роль в регуляции нормального гемопоэза. Мононуклеары могут ингибировать гемопоэз с помощью межклеточных взаимодействий и посредством выделения различных иммунных и не иммунных гуморальных факторов. 4. Образование клеток Моноцитарного ростка может происходить на любом этапе дифференциации от полипотентной стволовой кроветворной клетки до промиелоцита. Отличаются ли друг от друга Моноциты и Макрофаги, образовавшиеся из различных субпопуляций и каковы их специфические функции, пока не ясно. 5. Костномозговые Мононуклеары способны выходить из костного мозга в периферическую кровь, циркулировать в периферической крови по всему организму, проникать из кровеносного русла в любые органы и ткани и мигрировать в них – перемещаться в межклеточном пространстве. 6. Мононуклеар периферической крови в нормальных условиях созревает, перед тем как проникнуть в ткани, но при воспалении сроки пребывания его в периферической крови значительно сокращены, поэтому в ткани проникают его не зрелые формы, способные к активной пролиферации. 7. Тканевые Мононуклеары, это единственные клетки в организме человека, которые в нормальных условиях могут трансформироваться в другую бластную клетку – макрофаальный бласт с последующей дифференцировкой в Макрофаг. 8. Мононуклеар периферической крови, попадая в ткани, не обязательно трансформируется в Макрофаг, он может превратиться и в клетки микроокружения, например, в эпителиоидную клетку (мезенхимально-эпителиальный переход). 9. Будучи гистогенетически единой, кроветворная система в своем функционировании характеризуется определенной независимостью поведения отдельных ростков кроветворения, поэтому изначально Мононуклеары характеризуются независимостью поведения – автономностью. 10. Мононуклеары сохраняют способность к делению на всех этапах своего развития и имеют возможность трансформироваться в первичную стволовую злокачественную клетку. 11. Злокачественные клетки, подобно Мононуклеарам, обладают многими активными свойствами: влияют на пролиферацию, дифференцировку и функциональную активность различных клеток; выработку факторов роста; размножение в геле без подложки; сниженную адгезию; пониженное контактное торможение; влияние на гемопоэз; влияние на свертывающую систему крови; влияние на клеточный и гуморальный иммунитет и др. Таким образом, тканевые Мононуклеары (Промоноцит и Моноцит), вполне могут претендовать на роль «общего начала» или клетки-предшественницы первичной стволовой злокачественной клетки солидных опухолей. 4. ГЕНОТИПИЧЕСКИЕ ИЗМЕНЕНИЯ КОСТНОМОЗГОВОГО МОНОНУКЛЕАРА Мононуклеар, как и любая соматическая клетка, состоит из трех основных компонентов: клеточной мембраны, цитоплазмы и ядра (Рис. 9).
Рис. 9. Обобщенная схема животной клетки (Н. Грин, У. Стаут, Д. Тейлор, 1990, Т.1, стр. 211): 1 – митохондрии, 2 – цитоплазма, 3 – питательные гранулы, 4 – аппарат Гольджи, 5 – клеточная мембрана, 6 – центриоль, 7 – кариоплазма, 8 – ядрышко, 9 – хроматин, 10 – ядерная мембрана, 11 – лизосомы, 12 – секреторные гранулы. Характеристика ядра клетки Ядро – наиболее важная структура клетки, в нем сосредоточена основная масса ДНК, являющаяся носителем генетической информации. Кроме того, ядро регулирует всю «повседневную» жизнедеятельность клетки. Содержимое ядра: 1. Хромосомы, в которые входит фактически вся ДНК ядра, видны как дискретные тела, когда клетка находится на стадии активного деления. В состоянии покоя в периоды между делениями клетки (интерфаза) хромосомы могут быть не видны. 2. Ядрышко – особое тельце, в котором сосредоточена большая часть РНК в покоящемся или интерфазном ядре. 3. Ядерная плазма (кариоплазма) – это жидкость, содержащая соли и белки, но не содержащая нуклеиновых кислот. Ядро ограничено ядерной мембраной (кариолеммой), состоящей из двух липопротеидных слоев. Наружная мембрана связана с рибосомами, а к внутренней – тесно прилежит хроматин кариоплазмы. Наружная и внутренняя мембраны сливаются в области ядерных пор, через которые осуществляется транспорт белков и РНК. Поры ядерной мембраны заполнены белковым конгломератом, который изолирует кариоплазму от цитоплазмы, поэтому состав кариоплазмы, в том числе по содержанию ионов, отличается от состава цитоплазмы. Ген – это участок ДНК, содержащий программу построения только одного определенного белка по формуле «Один ген – один белок». Информация, содержащаяся в гене, передается в цитоплазму посредством матричной, или информационной РНК. Если контакт ядра с цитоплазмой прекращается, то скорость всех реакций в клетке постепенно замедляется, и она погибает. В период деления происходит «ремонт», воспроизведение и удвоение молекул ДНК, что позволяет передать дочерним клеткам одинаковый в количественном и качественном отношении объем генетической информации. Инициация костномозгового Мононуклеара Miller E., Miller J. (1966): предложили модель онкогенеза, в последствие названную, как «теория молекулярно-генетических механизмов многостадийного канцерогенеза». Процесс происходит в две стадии: инициации и промоции. Мы считаем, что предложенная «теория молекулярно-генетических механизмов многостадийного канцерогенеза» в действительности является только частью периода «зарождения» первичной стволовой злокачественной клетки. Тогда как модель онкогенеза включает в себя более широкое толкование, о чем будет изложено ниже. 1-я стадия (инициации от лат. initium – начало) периода «зарождения» стволовой злокачественной клетки: под канцерогенным воздействием (ионизирующее излучение, эндо- и экзоканцерогены, вирусы) наряду с относительно нейтральными повреждениями генома, могут происходить значимые мутации в онкогенах и антионкогенах. При этом возникает характерный спектр нарушений на генном, хромосомном и геномном уровнях: амплификации (увеличение копийности генов), делеции, инсерции, транслокации, микромутации (точковые замены, микроделеции, микроинсерции) и др. Важными положениями 1-ой стадии (инициации) являются: 1. Воздействие инициатора первично. 2. Доза инициатора влияет на частоту «зарождения» злокачественной клетки. 3. Инициация необратима. 4. Инициатор может быть применен однократно и кратковременно. 5. Инициатор воздействует самостоятельно. Известно, что генотипические изменения ядерной ДНК наиболее часто возникают в процессе митоза в зоне активной пролиферации. В организме человека наиболее интенсивная пролиферация происходит в красном костном мозге, и здесь сохранился наиболее недифференцированный состав стволовых клеток, приближенных к эмбриональным. Интенсивность пролиферации в красном костном мозге может значительно возрастать при хроническом воспалении. Это увеличение отмечается в костном мозге, периферической крови, селезенке, лимфатических узлах, перитонеальных полостях. При ускоренной пролиферации образование клеток Моноцитарной серии может происходить на любом этапе дифференциации от полипотентной стволовой кроветворной клетки до Промиелоцита. Отличаются ли друг от друга Моноциты и Макрофаги, образовавшиеся из различных субпопуляций клеток-предшественников и каковы их специфические функции – не известно. Генотипические изменения ядерной ДНК Boveri T. (1914): в основе малигнизации лежит мутация, возникающая под влиянием эндогенных и экзогенных канцерогенных веществ и облучения. Во время усиленной пролиферации при стимулированном гемопоэзе, под канцерогенным воздействием (ионизирующее излучение, эндо- и экзоканцерогены, вирусы), в клетке во время митоза может проявиться свойство «геномной нестабильности». Наряду с относительно нейтральными повреждениями генома, могут происходить значимые мутации в онкогенах и антионкогенах. При этом возникает инициированная клетка, имеющая характерный спектр нарушений на генном, хромосомном и геномном уровнях: амплификации (увеличение копийности генов), делеции, инсерции, транслокации, микромутации (точковые замены, микроделеции, микроинсерции) и др. Генотипические изменения могут возникнуть на различной стадии гемопоэза и чем выше согласно схеме кроветворения, тем большей потентностью будет обладать стволовая злокачественная клетка. Поэтому важно знать не только какие возникли генотипические изменения ядерной ДНК, но и на каком уровне гемопоэза они возникли, т.е. важен не только характер генотипических изменений (спектр нарушения) ядерной ДНК, но и уровень генотипических изменений (класс по схеме кроветворения). Как было сказано выше, все стадии гемопоэза подразделяют на шесть основных классов. В каждом конкретном случае при канцерогенном воздействии возникают различные генотипические изменения ядерной ДНК, но только на одном из вышеуказанных классов гемопоэза. Для «зарождения» стволовой злокачественной клетки солидных опухолей наиболее вероятными являются следующие уровни потентности: 1. II класс – полипотентная клетка-предшественница родоначальница миелопоэза, общая для 4 ростков (КОЕ-ГЭММег) с последующим развитием в направлении Моноцитарного ростка. 2. III класс – унипотентная клетка-предшественница родоначальница Моноцитов (КОЕ-М). Необходимо подчеркнуть, что генотипические изменения ядерной ДНК, происходят по рецессивному признаку, поэтому в красном костном мозге эти изменения никоим образом себя не проявляют. В процессе дифференцировки, генотипические изменения закладываются в генетическом аппарате будущего Промоноцита и Моноцита, которые морфологически не отличается от нормального костномозгового Мононуклеара. Существует еще генетический или наследственный путь передачи генотипических изменений ДНК ядра клетки, когда «кровным» родственникам в 1–15% случаев передается предрасположенность к развитию злокачественного заболевания. В этом случае генотипические изменения ядерной ДНК костномозгового Мононуклеара уже имеются и канцерогенное воздействие не обязательно или является пусковым механизмом для их реализации. Приобретение генотипических изменений ядерной ДНК для Мононуклеара не является решающим в возможности трансформации в стволовую злокачественную клетку. Генотипически измененный Мононуклеар может делиться (митоз), созревать, дифференцироваться, преобразовываться в клетки микроокружения, трансформироваться в Макрофаг. И хотя необратимые генотипические изменения Мононуклеара являются абсолютной необходимостью, для трансформации в стволовую злокачественную клетку этого совершенно недостаточно. Генотипические изменения ДНК ядра Мононуклеара будут терпеливо ждать до тех пор, пока не возникнут оптимальные условия для их проявления и тогда «зародившиеся» потомки – стволовые злокачественные клетки, будут властвовать в организме-носителе. Но для «зарождения» стволовой злокачественной клетки, еще необходимы эпигенетические изменения, которые могут происходить, только если клетка окажется в определенном микроокружении, характеризующимся, как «суперусловия». Таким образом, в красном костном мозге при канцерогенном воздействии во время ускоренного гемопоэза может возникнуть инициированная клетка, имеющая различные генотипические изменения ядерной ДНК. |